新聞中心 / News Center
贝达药业BPI-21668获批开展临床试验
日期: 2021-03-03

3月3日,贝达药业收到国家药品监督管理局签发的《药物临床试验批准通知书》(通知书编号:2021LP00274、2021LP00275),公司申报的BPI-21668片用于治疗晚期实体瘤的药品临床试验申请已获得国家药品监督管理局批准。
BPI-21668是一个由贝达药业自主研发的拥有完全自主知识产权的新分子实体化合物,是一种新型强效、高选择性的磷脂酰肌醇3-激酶α(Phosphatidylinositol 3-kinase α, PI3Kα)口服小分子抑制剂,拟用于PIK3CA(Phosphatidylinositol-4,5-bisphosphate 3-kinase catalytic subunit alpha)基因突变的晚期实体瘤的治疗。
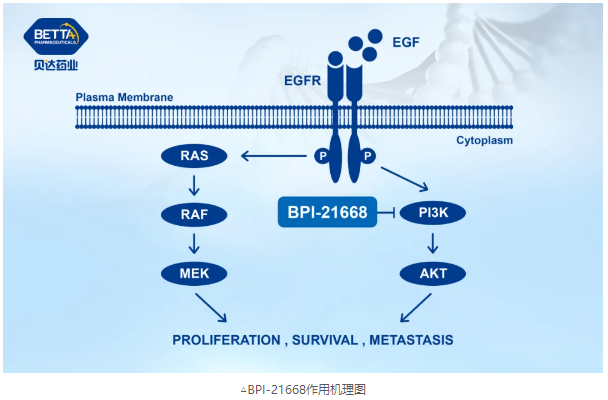
目前,全球仅有一款PI3Kα选择性抑制剂Alpelisib获批用于携带PIK3CA突变的HR+/HER2-乳腺癌治疗,中国区域内尚无PI3Kα选择性抑制剂上市。BPI-21668属于“境内外均未上市的创新药”,其注册分类为化学药品1类。
下一条: 恩沙替尼II期研究动态ctDNA分析结果在JTO发表
热门点击

